Diméthylsilane
| Diméthylsilane | |
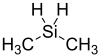 Structure du diméthylsilane |
|
| Identification | |
|---|---|
| Nom UICPA | diméthylsilane |
| No CAS | |
| No ECHA | 100.012.895 |
| No CE | 214-184-7 |
| PubChem | 66185 |
| SMILES | |
| InChI | |
| Apparence | gaz incolore à l'odeur douceâtre et nauséeuse |
| Propriétés chimiques | |
| Formule | C2H8Si [Isomères] |
| Masse molaire[1] | 60,170 4 ± 0,002 5 g/mol C 39,92 %, H 13,4 %, Si 46,68 %, |
| Propriétés physiques | |
| T° fusion | −150,2 °C[2] |
| T° ébullition | −19,6 °C[2] |
| T° d'auto-inflammation | 205 °C[2] |
| Point d’éclair | −30 °C[2] |
| Limites d’explosivité dans l’air | entre 1,2 % vol. et 74,0 % vol.[2] |
| Pression de vapeur saturante | 380 kPa[2] à 20 °C |
| Précautions | |
| SGH[2] | |
| H220 et H280 |
|
| Transport[2] | |
| Unités du SI et CNTP, sauf indication contraire. | |
Le diméthylsilane est un composé chimique de formule SiH2(CH3)2. Gaz incolore pyrophorique à l'odeur douceâtre et nauséeuse, il est très inflammable — point d'éclair inférieur à −30 °C et point d'auto-inflammation de 205 °C — et forme des mélanges explosifs avec l'air, ses limites d'explosivité étant de 1,2 % et 74 % en volume, soit une concentration de 30 à 1 851 g/m3.
Le diméthylsilane s'hydrolyse dans l'eau et les acides en donnant du diméthylsilanediol Si(OH)2(CH3)2 et de l'hydrogène H2, qui s'enflamme souvent immédiatement.
Il peut être obtenu en quantité par l'action du dichlorosilane SiH2Cl2 sur du diméthylzinc Zn(CH3)2 gazeux, réaction qui donne également du chlorure de méthylzinc ClZnCH3[3] :
On peut également le produire en réduisant du diméthyldichlorosilane SiCl2(CH3)2 avec un réducteur approprié, comme l'aluminohydrure de lithium LiAlH4.
Il est utilisé en dépôt chimique en phase vapeur (CVD) dans l'industrie des semi-conducteurs, par exemple pour la production de diélectriques low-κ [4].
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Dimethylsilane » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 15 décembre 2012 (JavaScript nécessaire)
- ↑ (de) Alfred Stock et Carl Somieski, « Siliciumwasserstoffe VI.: Chlorierung und Methylierung des Monosilans », Berichte der deutschen chemischen Gesellschaft (A and B Series), vol. 52, no 4, , p. 695-724 (DOI 10.1002/cber.19190520410, lire en ligne)
- ↑ (en) Qingguo Wu et Karen K. Gleason, « Plasma-enhanced chemical vapor deposition of low-k dielectric films using methylsilane, dimethylsilane, and trimethylsilane precursors », Journal of Vacuum Science & Technology A, vol. 21, no 2, , p. 388 (DOI 10.1116/1.1539086, Bibcode 2003JVST...21..388W, lire en ligne)



